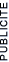La masse moléculaire relative
I. Masse moléculaire relative
I.1. Définition
La masse moléculaire relative d'une molécule est le rapport entre la masse de cette molécule et le douzième de la masse de l'isotope 12 du carbone, choisi comme masse de référence
Approximation (3e secondaire)
La masse moléculaire relative d'une molécule est le rapport entre la masse de cette molécule et la masse d'un atome d'hydrogène (H), choisie comme masse de référence. I.2. Notation
II. Calcul de la masse moléculaire relative
La masse moléculaire relative d'une molécule se calcule en additionnant la masse atomique relative de tous les atomes qui composent cette molécule.
Exemple
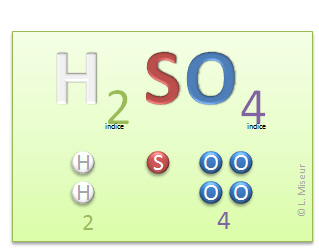
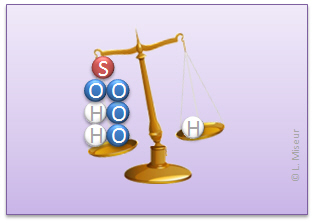
Formellement : Ar(H) + Ar(H) +Ar(S) + Ar(O) + Ar(O) + Ar(O) + Ar(O)
ce qui se calcule également directement grâce aux indices :
2 . Ar(H) = 2 . 1, car il y a deux atomes d'hydrogène qui constituent une molécule de ce composé
+ 1 . Ar(S) = 32
+ 4 . Ar(O) = 4 . 16, car il y a quatre atomes d'oxygène qui constituent une molécule de ce composé
= 2 . 1 + 32 + 4. 16 = 98
Dans notre exemple Mr H2SO4 = 98
![]() Cette masse
est la masse moléculaire relative de la molécule comparée à la masse de la douzième partie de
l'isotope 12 du carbone.
Cette masse
est la masse moléculaire relative de la molécule comparée à la masse de la douzième partie de
l'isotope 12 du carbone.
Calcul la masse moléculaire relative des molécules suivantes :
[Quelques masses atomiques relatives : H=1; Fe=56 ; O=16 ; Na=23; Cl=35; K=39 ; Mn=55 ; I=127]
HCl (Chlorure d'hydrogène) : Mr = KMnO4 (Permanganate de potassium): Mr = Fe2O3 (Oxyde de Fer III) : Mr = I2 (diiode): Mr = NaCl (Chlorure de sodium) : Mr =
![]()
| ||||||